AbstractObjectives:Smoking is an important risk factor for metabolic syndrome (Mets) and cardiovascular disease. This study has been designed to investigate the relationship between smoking, metabolic syndrome, and arteriosclerosis among men in South Korea.
Methods:We have retrospectively enrolled data of 5,103 men aged over 20 years, who underwent a health check-up including carotid ultrasonography in 2014. Smoking status and amount were collected from self-reported questionnaires. The diagnosis of Mets was made using criteria modified NCEP-ATP III. Using multivariate logistic regression analysis, the risk of Mets and arteriosclerosis defined as abnormal carotid intima-media thickness (CIMT) and carotid plaque according to smoking amounts was examined.
Results:Both former (29.7%) and current (27.8%) smokers had a higher prevalence of Mets than never (23.2%) smokers [OR (95% CI): former, 1.35 (1.14, 1.6); current, 1.63 (1.35, 1.98), respectively]. There had been a significant increase in the risk of Mets, low HDL-cholesterol and high fasting blood sugar among the former and current smokers who smoke ≥ 20 pack-years (PY) (p < 0.001). And there had also been a significant increase in the risk of high triglyceride at all levels in smoking amount. There was a clear dose-dependent relationship between smoking amount and arteriosclerosis especially the risk of carotid plaque (all p < 0.005). In individuals without Mets, smoking consumption in former or current smokers was positively associated with the risk of CIMT and carotid plaque by adjusted age, BMI, LDL-cholesterol.
서 론흡연은 심혈관계질환의 주요 위험인자이다[1]. 이에 대한 기전은 명확하지 않지만, 흡연이 인슐린 저항성을 증가시키고 이러한 인슐린대사의 변화가 심혈관계 질환 위험을 가속화시킨다고 알려져 있다[2]. 복부비만, 혈당이상, 고혈압, 이상지질혈증 등 대사적 이상의 조합으로 정의되는 대사증후군의 경우, 인슐린 저항성이 증가하여 당뇨병 혹은 심혈관계 질환의 발생 가능성이 높아진다[3]. 이러한 특징은 흡연이 대사증후군 발생위험을 증가시킴으로써 심혈관계 질환의 위험을 증가시킬 가능성을 시사한다[4,5]. 또한 흡연은 대사증후군 구성인자 중 고밀도 콜레스테롤을 낮추고 중성지방을 높일 뿐 아니라, LDL 콜레스테롤(low-density lipoprotein cholesterol) 수치를 높이며, 심혈관계 질환의 위험을 증가시키는 위험요인으로 작용한다[6,7]. Copenhagen 남성을 8년 간 추적한 조사에서는 흡연자에게 인슐린대사의 변화가 있었으며, 이 중 중성지방과 고밀도 콜레스테롤 변화 등 지질대사 이상을 동반한 경우 심혈관계 질환 위험이 높다고 밝혔다[8]. Ishizaka et al. [9]은 흡연 상태에 따른 대사증후군 유병률을 비흡연자 8.8%, 과거흡연자 20.4%, 현재흡연자 23.7%로 보고하여, 흡연경험과 대사증후군 위험의 관련성을 설명하였다. 또한 Hong et al. [10]의 연구에서, 비흡연자에 비해 과거 및 현재흡연자는 약 2배 이상 높은 대사증후군 위험을 보였다.
대사증후군 위험과 흡연자의 누적흡연량은 용량반응적 관계를 갖는다[11]. 대사증후군 위험을 증대시키는 누적흡연량 수준은 연구마다 차이가 있으며, 그 범위는 10갑년 이상에서 30갑년 이상까지 다양하다[9,11,12]. 흡연은 신체활동, 식이, 음주 등과 함께 대사증후군의 개선 가능한 위험요인으로 간주되며, 이러한 이유로 흡연을 중단하여 대사증후군 위험을 낮출 것을 권고하였다[13,14]. 그러나 기존 연구는 대부분 현재흡연자로 한정하여 보고되고 있어, 흡연 중단자의 금연 전 누적흡연량에 따른 질환위험 수준을 정의하는 데 한계가 있다.
심혈관계 질환의 위험요인으로 흡연과 대사증후군은 매우 중요하다. 중국인을 대상으로 한 Zhang et al. [15]의 연구는 대사증후군과 흡연요인에 따른 심혈관계 질환 위험도를 설명하는 데 있어, 두 요인이 모두 있는 집단에서 가장 높은 위험을 보였으며, 그 수준은 그렇지 않은 집단에 비해 17.41배 높다고 하였다. 또한 심혈관계 질환 위험도를 대사증후군과 흡연자의 누적흡연량 수준에 따라 평가한 He et al. [16]의 연구에서 용량 반응적 관계를 확인하였다.
그러므로 본 연구는 높은 흡연율을 보이는 한국 남성을 대상으로, 과거흡연 및 현재흡연자에서 흡연 상태뿐만 아니라 흡연의 수준에 따른 대사증후군 및 심혈관계 질환 위험도를 가늠하는 동맥경화증과의 관련성을 확인하고자 하였다. 또한 흡연이 동맥경화증의 위험요인으로 작용함에 있어서 대사증후군이 어떤 역할을 하는지 그 관련 특성을 알아보고자 하였다.
연구 방법연구 대상2014년 1월부터 12월까지 서울 소재의 한 건강증진센터에서 경동맥 초음파검사를 포함하여 건강검진을 실시한 20세 이상 성인 남성을 대상으로 하였다. 이 중 뇌졸중 혹은 심장병으로 약을 복용하는 경우와 흡연 관련 문항에 응답하지 않거나, 신체계측을 포함한 필요 검사를 받지 않은 경우를 제외하여, 최종 5,103명을 대상자로 포함하였다. 본 연구는 한국건강관리협회 IRB 위원회의 승인을 받았다(IRB No. 130750-201510-HR-025).
연구 방법흡연습관 및 질환력자기기입식 설문조사방법을 활용하여 흡연습관과 질환력을 조사하였으며, 흡연상태와 함께 과거 및 현재흡연자의 흡연기간과 용량을 조사하였다. ‘평생 총 5갑(100개비) 이상의 담배를 피운 적이 있는가’에 대하여 지금은 끊은 경우를 과거흡연자, 현재도 흡연중인 경우를 현재 흡연자, 담배를 피운 경험이 없는 경우를 비흡연자로 분류하였다. 과거 및 현재흡연자의 담배 소비량(갑년, pack-year)은 [총 흡연량(개비)/20]×[흡연기간(년)]으로 계산하였으며, 과거흡연자는 금연 전까지의 정보를 활용하였다. 이는 20갑년을 장기흡연 기준으로, 20갑년 미만, 20-40갑년 미만, 40갑년 이상으로 구분하였다[17].
질병을 진단받아 현재 약물치료를 받고 있는지를 조사하였다. 뇌졸중과 심장병으로 약물치료를 받는 경우는 제외하였으며, 고혈압, 당뇨병, 이상지질혈증으로 약물치료 받는 경우는 대사증후군의 각 해당요소로 분류하였다.
신체계측 및 혈압체질량지수(body mass index, BMI)는 체중(kg)/신장(m)2로 계산하였으며, 신장과 체중은 신발과 양말을 벗고 직립자세에서 자동신체계측기로 측정하였다. 허리둘레는 늑골하단과 골반 장골 능 상단 사이의 중간지점에서 줄자로 측정하였다. 혈압은 5분 이상 안정 상태를 유지한 후 자동혈압계로 측정하였으며, 수축기혈압 ≥140 mmHg 이거나 이완기혈압 ≥ 90 mmHg인 경우 수은혈압계로 다시 측정하였다.
혈액 화학검사 및 대사증후군채혈 전 10시간 공복을 유지하였으며, Hitachi 7600 (Hitachi, Nakai, Japan)을 활용하여 혈액의 혈청에서 공복혈당, 중성지방, HDL 콜레스테롤(high density lipoprotein cholesterol), LDL 콜레스테롤을 측정하였다. 혈당, 중성지방, HDL 콜레스테롤은 아산시약(Asan Inc., Hwaseong, Korea)을, LDL 콜레스테롤은 Daiichi 시약(Daiichi Pure Chemicals Co., Tokyo, Japan)을 사용하였으며, 모두 효소법으로 측정하였다. 지질검사의 정밀도와 정확도는 정도관리 물질인 Lyphocheck levels Ⅰ, Ⅱ (Bio-Rad Lab., Irvine, USA)를 사용하여 평가하였으며, 대한임상검사정도관리협회 정도관리사업에 참여하였다.
National Cholesterol Education Program Adult Treatment Panel III(NCEP-ATPIII)의 진단기준을 수정하여, 2005년 미국심장협회와 국립심폐혈관연구소에서 제시한 modified ATP Ⅲ를 적용하여 대사증후군을 정의하였다[18]. 허리둘레, 혈압, 공복혈당, 중성지방, HDL 콜레스테롤 등 5개 대사 항목 중 3개 이상이 해당 범위에 포함되면 대사증후군으로 진단하였다. 대사증후군의 항목별 범위는 허리둘레의 경우 아시아인의 복부비만 기준인 ≥ 90 cm를 적용하였으며[19], 수축기혈압 ≥130 mmHg 또는 이완기혈압 ≥85 mmHg를 고혈압 이상, 공복혈당 ≥ 100 mmHg, 중성지방 ≥150 mmHg, HDL 콜레스테롤 <40 mg/dL을 각 항목별 해당 범위로 적용하였다. 고혈압, 당뇨병, 이상지질혈증으로 약물을 복용하는 경우는 각 해당 항목이 있는 것으로 정의하였다.
경동맥 두께 및 동맥경화반 측정죽상경화는 심혈관질환의 원인으로 알려져 있으며, 대표적으로 경동맥초음파검사를 통해 경동맥 내중막 두께와 동맥경화반을 측정하여 진단한다. 경동맥 상태는 B-mode 초음파기(SONOACE 9900, Medison, Korea)의 7.5 MHz 선상 탐촉자(linear ultrasound transducer)를 사용하여 측정하였다. 경동맥 내중막 두께의 측정은 혈관 내강과 내막의 경계 부위로부터 혈관중막과 외막의 경계 부위까지의 거리로 정의한다.
비정상 경동맥 내중막 두께(abnormal carotid intima-media thickness, Abnormal CIMT)는 경동맥 내중막 두께 1 mm를 기준으로 그 이상인 경우로 정의하며, 동맥경화반은 인접한 내중막 두께보다 100% 이상 혈관 내강 쪽으로 돌출된 경우로 정의한다.
통계분석일반적 특성을 포함하여, 임상 및 대사적 특성을 평균과 표준편차로 요약하여 제시하였고, 흡연상태에 따른 차이를 비교하기 위해 일원분산분석(one-way ANOVA)을 실시였으며, 사후비교(posthoc comparison)는 Scheffe’s method를 활용하였다. 비정상 경동맥 내중막 두께, 동맥경화반의 분포와 대사증후군 및 개별 대사이상 인자별 분포는 빈도와 비율로 요약하였으며, 흡연상태에 따른 차이는 χ2 검정을 실시하여 통계적으로 유의한 차이가 있는지를 분석하였다.
누적흡연량을 포함한 흡연상태에 따른 대사증후군 및 개별 대사인자 이상, 비정상 경동맥 내중막 두께, 동맥경화반 유무 등의 관련성을 알아보기 위해, 연령, BMI를 보정한 다중로지스틱 회귀분석을 실시하였다. 오즈비(odds ratio, OR)와 95% 신뢰구간(confidence interval, CI)을 제시하였으며, 오즈비의 선형 경향성(linear trend)을 확인하기 위해 경향분석(test for trend)을 실시하였다. 흡연과 비정상 경동맥 내중막 두께 및 동맥경화반 유무의 관련성을 알아보기 위하여, 대사증후군 유무로 나누어 연령, BMI, LDL 콜레스테롤을 보정한 다중로지스틱 회귀분석을 실시하였다. 본 연구의 통계분석은 SAS 9.3 프로그램(SAS Institute Inc., Cary, NC, USA)을 사용하였으며, 유의수준 0.05를 기준으로 분석하였다.
연구 결과본 연구 대상자 5,103명 중 과거흡연과 현재흡연 경험률은 각 41.5% (2,115명), 30.5% (1,555명)로, 10명 중 7명이 흡연을 경험하였다. 대상자의 평균연령은 과거흡연자 57.84±10.18세로 가장 높았으며, 비흡연자, 현재흡연자 순으로 나타났다(p < 0.001). BMI와 허리둘레의 평균수치는 과거흡연자가 비흡연자에 비해 높은 수준을 보였다(각 p = 0.004, p = 0.001). 평균 수축기혈압은 흡연상태에 따라 유의한 차이를 보여, 비흡연자에 비해 과거흡연자는 높고 현재흡연자는 낮은 데 비해, 평균 이완기혈압은 비흡연자에 비해 현재흡연자가 낮은 수준을 보였다(각 p < 0.001).
중성지방의 평균수치는 현재흡연자, 과거흡연자, 비흡연자 순으로 유의한 차이를 나타냈으며, HDL 콜레스테롤의 평균수치는 비흡연자와 과거흡연자가 유의한 차이를 보이지 않는 데 비해, 현재흡연자는 유의하게 낮은 수준이었다(각, p < 0.001). 총콜레스테롤 평균수치는 현재 흡연자가 가장 높았으며, 비흡연자와 과거흡연자는 유의한 차이를 보이지 않았다(p < 0.001). 공복혈당의 평균수치는 과거흡연자가 비흡연자보다 유의하게 높았다(p = 0.009). 비정상 경동맥 내중막 두께 비율은 과거흡연자 68.4%, 비흡연자 61.2%, 현재흡연자 55.9% 순으로 유의한 차이를 보였다(p < 0.001). 동맥경화반의 비율은 과거흡연자가 52.4%로 현재흡연자 44.9%와 비흡연자 44.0%에 비해 유의하게 높은 수준을 보였으며(p < 0.001), 현재흡연자와 비흡연자 간 비슷한 수준을 보였다(Table 1).
본 연구에서 대사증후군 유병률은 27.3%였으며, 흡연상태에 따라 과거흡연자가 29.7%로 가장 높았고, 현재흡연자 27.8%, 비흡연자 23.2%로 비흡연자가 가장 낮은 수준이었다(p < 0.001). 대사증후군 위험인자의 평균 개수는 과거흡연자(1.86±1.25개), 현재흡연자(1.74±1.30개), 비흡연자(1.63±1.26개) 순으로 높았다(p < 0.001). 대사증후군의 5가지 구성요인별 이상범위 포함 비율은 저 HDL 콜레스테롤 14.3%이며, 복부비만 29.9%, 고 중성지방혈증 33.4%, 공복혈당이상 43.7%, 고혈압 54.6%이었다. 대사증후군 위험인자 중 HDL 콜레스테롤을 제외한 모든 요인의 이상범위에 포함된 비율은 흡연상태에 따라 유의한 차이를 보였다. 허리둘레 기준의 복부 비만율은 과거흡연과 현재흡연에서 각 31.9%, 29.7%로, 비흡연에 비해 높게 나타났다(p = 0.008). 고혈압과 공복혈당 이상 비율은 과거흡연자에서 유의하게 높은 데 비해(각, p < 0.001), 고중성지방혈증 비율은 현재흡연자에서 40.6%로 가장 높았다(p < 0.001).
연령과 BMI를 보정한 흡연상태에 따른 대사증후군의 오즈비는 비흡연자에 비해 흡연 경험이 있는 경우 높았으며, 특히 현재흡연자에서 가장 높았다[OR (95% CI): 과거흡연자 1.35 (1.14, 1.6), 현재흡연자 1.63 (1.35, 1.98)]. 대사증후군 구성인자 가운데 고 중성지방혈증과 공복혈당 이상 위험도는 흡연수준이 심각할수록 높았으며, 특히 고 중성지방혈 증은 비흡연자에 비해 현재흡연자의 위험도가 1.95배(95% CI: 1.66, 2.30)였다. 허리둘레 기준 복부비만 위험과 저 HDL 콜레스테롤 위험은 비흡연자에 비해 과거흡연자는 유의한 차이를 보이지 않은 데 비해, 현재흡연자는 유의하게 높았다[OR (95% CI): 복부비만 1.31 (1.04, 1.65), 저 HDL 콜레스테롤 1.42 (1.15, 1.76)]. 고혈압의 오즈비는 비흡연자에 비해 현재흡연자가 0.84배(95% CI: 0.72, 0.99)로 낮게 나타났다(Table 2).
흡연의 양에 따른 대사증후군의 오즈비는 과거흡연자와 현재흡연자 모두 20갑년 이상에서 비흡연자에 비하여 통계적으로 유의한 차이를 보였다. 특히 같은 흡연량 수준에서 비교할 때, 대사증후군 위험은 과거흡연자 보다 현재흡연자에서 높았다. 흡연량이 20-40갑년 미만인 경우의 대사증후군 위험은 비흡연에 비해 과거흡연자가 1.83배(95% CI: 1.47, 2.27), 현재흡연자가 1.94배(95% CI: 1.53, 2.48)였으며, 40갑년 이상의 높은 흡연량에서는 과거흡연자가 1.55배(95% CI: 1.07, 2.24), 현재 흡연자가 2.01배(95% CI: 1.45, 2.78)로 차이를 보였다. 대사증후군 위험인자 중 허리둘레 기준 복부비만의 위험은 현재흡연자 중 20갑년 이상의 흡연량을 가진 경우 높았다. 저 HDL 콜레스테롤혈증과 공복혈당 이상의 위험은 과거흡연자와 현재흡연자 모두 비흡연자에 비해 20갑년 혹은 40갑년 이상의 높은 흡연량을 경험한 경우 유의하게 높았다. 고 중성지방혈증 위험은 흡연량이 많을수록 유의하게 높았으며, 과거 흡연자보다 현재흡연자에서 높은 오즈비를 보였다. 고혈압을 제외한 대사증후군 위험인자는 모두 흡연량에 따라 유의한 경향을 보였다(p < 0.05 for trend).
비정상 경동맥 내중막 두께의 위험은 비흡연자에 비해 20갑년 미만 흡연한 현재흡연자가 1.3배(95% CI: 1.02, 1.63) 높았으며, 20갑년 이상 흡연한 현재흡연자는 약 1.5배 높은 수준을 보였다[OR (95% CI): 20-40갑년 1.54 (1.23, 1.94), 40갑년 이상 1.48 (1.04, 2.11)]. 과거 혹은 현재흡연자 모두 흡연량이 증가함에 따라 동맥경화반 위험은 유의하게 높아지는 특징을 보였다(p < 0.005 for trend). 과거흡연자는 흡연량 20갑년을 기준으로 동맥경화반 위험수준이 높아졌으며, 현재흡연자는 흡연량과 비례하는 위험도를 보였다. 특히 40갑년 이상 흡연량을 경험한 현재 흡연자의 동맥경화반 위험수준은 비흡연자에 비해 2.20배(95% CI: 1.62, 3.01)로 높았다(Table 3).
흡연상태에 따른 죽상동맥경화증 위험도는 연령, BMI, LDL 콜레스테롤을 보정한 후, 대사증후군 유무로 나누어 살펴보았다. 비정상 경동맥 내중막 두께의 위험도는 대사증후군이 없는 경우 비흡연자에 비해 현재흡연자가 1.30배(95% CI: 1.05, 1.60) 높은 수준이며, 대사증후군이 있는 경우 흡연상태에 따른 차이를 보이지 않았다. 동맥경화반 위험도는 대사증후군이 없는 경우와 있는 경우 모두 흡연상태에 따라 유의한 차이를 보였으며, 흡연상태가 심각할수록 위험도가 높아졌다[OR (95% CI): 대사증후군이 없는 경우 과거흡연 1.35 (1.13, 1.62)와 현재흡연 1.74 (1.42, 2.12), 대사증후군이 있는 경우 과거흡연 1.36 (1.00, 1.85)과 현재흡연 1.67 (1.19, 2.35)] (Figure 1).
비정상 경동맥 내중막 두께의 오즈비는 대사증후군이 없는 경우, 과거흡연과 현재흡연 모두 흡연량이 20-40갑년 미만군에서 유의하였으며, 비흡연 보다 높은 위험을 보였다[20-40갑년 미만군의 OR (95% CI): 과거흡연 1.38 (1.04, 1.83), 현재흡연 1.44 (1.11, 1.88)]. 대사증후군이 있는 경우는 흡연 상태 및 양에 따른 비정상 경동맥 내중막 두께의 위험도가 유의하지 않았다(Figure 2).
대사증후군이 없는 경우, 과거흡연자와 현재흡연자의 흡연량이 많을수록 동맥경화반 위험이 높았다. 과거흡연자의 오즈비는 흡연량이 20갑년 이상에서 유의하였으며, 약 1.7배의 높은 위험도를 보였다[OR (95% CI): 20-40갑년 미만 1.67 (1.31, 2.14), 40갑년 이상 1.69 (1.09, 2.63)]. 현재흡연자는 흡연량에 따라 동맥경화반 위험도가 비례적으로 증가하여, 흡연량이 많은 경우 높은 위험도를 보였다[OR (95% CI): 20갑년 미만 1.37 (1.06, 1.78), 20-40갑년 미만 1.89 (1.47, 2.43), 40갑년 이상 2.33 (1.59, 3.40)]. 대사증후군이 있는 경우는 동맥경화반 위험이 현재흡연자에서만 유의하였으며, 40갑년 미만의 흡연량인 경우 비흡연자에 비해 높은 위험도를 보였다[OR (95% CI): 20갑년 미만 1.86 (1.17, 2.96), 20-40갑년 미만 1.63 (1.07, 2.48)] (Figure 3).
고 찰성인남성 5,103명을 대상으로 실시한 본 단면연구에서, 대사증후군 위험은 비흡연에 비해 과거 혹은 현재흡연인 경우와 누적흡연량이 많을수록 증가하였다. 특히 20갑년 이상의 누적흡연량을 경험한 과거흡연자와 현재흡연자는 비흡연자에 비해 높은 대사증후군 위험을 보였다. 본 연구는 흡연량과 대사증후군 간의 관계에 있어, 과거흡연자와 현재흡연자가 비슷한 용량 수준에서 그 위험이 증가하는 결과를 보였다. 현재흡연자를 대상자로 한정한 기존 연구에서 누적흡연량이 증가할수록 대사증후군 위험이 비례적으로 증가하는 관련성을 보여주었다[11,12,20]. 또한 과거흡연자의 금연 전 누적흡연량과의 관계를 확인한 Ishizaka et al. [9]과 Wada et al. [21]의 연구에서 누적흡연량 수준이 10갑년과 20갑년 이상인 경우, 과거흡연자의 대사증후군 위험이 유의하게 높아진다고 하여, 본 연구와 유사한 결과를 보였다. 그러나 Chen et al. [22]은 과거흡연자는 대사증후군의 위험요인으로 유의하지 않다고 밝혀 본 연구와 차이가 있었다.
본 연구에서 20갑년 이상 흡연량을 경험한 과거흡연자는 여전히 대사증후군 위험이 증가하였다. 이는 금연 후에도 질환 위험이 쉽게 감소하지 않는 기존 연구결과와 일치한다[9,23,24]. 과거흡연자와 현재흡연자를 동일 누적흡연량 수준에서 비교할 때, 복부비만, 저 HDL 콜레스테롤혈증, 공복혈당 이상의 위험도가 비슷하게 나타났으나, 금연 지속기간을 반영하지 않은 본 연구에서 금연의 효과를 입증하는 데 한계가 있었다. 또한 과거흡연자의 대사증후군 위험도가 누적흡연량 40갑년 이상 보다 20-40갑년 미만에서 높은 특징을 보였으며, 이는 흡연과 질병의 용량반응적 관계를 고려하면 금연지속 기간의 차이에 기인한 것으로 추정된다. 이전 연구에서는 금연 기간이 짧은 단기 금연자가 체중증가와 인슐린 저항성이 지속되어 대사증후군 위험이 금연 후 쉽게 감소하지 않는다고 하였다[20,23,25,26]. 또한 금연에 따른 건강수준의 향상을 기대하기 위해서는 충분한 금연지속기간이 필요하다[27,28]. 금연효과가 나타나기 위한 금연기간은 연구자마다 차이가 있지만, 대체로 과거 누적흡연량이 많을수록 더 긴 금연기간이 필요하다고 하였다[24]. 실제 한 연구에서는 20갑년 이상 흡연경험이 있는 과거흡연자는 대사증후군 위험을 낮추기 위해 최소한 20년 이상 금연기간을 유지해야 한다는결과를 제시하였다[21].
흡연은 인슐린 저항성을 일으키고 교감신경활동을 증가시켜, HDL 콜레스테롤 감소와 중성지방 증가를 유도하는 등 지질대사에 영향을 미친다[14,29]. 이러한 변화는 대사증후군 발생을 유도하며, 관상동맥질환의 위험을 증가시킬 수 있다. 본 연구는 대사증후군 구성인자 중 고혈압을 제외한 복부비만, 저 HDL 콜레스테롤혈증, 고 중성지방혈증, 공복혈당 이상의 위험도가 누적흡연량 수준이 높은 경우 증가하는 것을 확인하였다. 이러한 특성은 과거흡연자와 현재흡연자 모두 동일하였으며, 특히 현재흡연자는 20갑년 이상에서 유의하게 대사증후군 위험이 증가하였다. 누적흡연량이 많을수록 고 중성지방혈증 위험도가 높아지는 비례적 관계는 현재흡연자에서 뚜렷하게 나타났다. 다양한 기존연구에서 흡연과 대사증후군 간의 관계를 설명하는 인자로서 HDL 콜레스테롤과 중성지방을 제시하였다[11,22]. 또한 일부 단면 연구에서 공복혈당 위험과 흡연수준 간의 유의한 결과를 도출하지 못하였으나[10,12,23], 공복혈당장애 혹은 제2형 당뇨병 발생률과 흡연량 간의 관련성을 규명한 다양한 종단연구는 본 연구와 일치하는 결론을 보였다[24,30]. 니코틴은 카테콜아민의 분비를 유도하여 혈압을 상승시키는 역할을 한다[31]. Minami et al. [32]은 흡연자의 혈압을 2주간 측정하는데, 1주는 흡연을 유지하여 측정하고 1주는 흡연을 중단하여 측정하였으며, 그 결과 비흡연 기간의 혈압이 흡연기간의 혈압보다 낮은 것을 확인하였다. 반면, 흡연여부가 혈압 간 유의한 차이를 발견하지 못한 이전 연구가 있다[28]. 일부 연구는 그 원인으로 흡연자들이 검진을 실시하기까지 단시간 흡연을 중단하였으며, 이것이 교감신경의 항진을 억제하였을 가능성을 제시하였다[23]. 본 연구에서도 흡연과 고혈압 간에 유의한 관계를 발견하지 못하였으나, 흡연이 영향요인으로 작용하지 않는다고 결론 내리기에는 논란이 있으며, 이를 규명하기 위한 추가적인 연구가 요구된다.
본 연구에서 대사증후군이 있는 경우 누적흡연량이 증가할수록 동맥경화반 위험이 높아졌으며, 이는 현재흡연자에서 더욱 뚜렷한 경향으로 나타났다. Reaven and Tsao [5]와 Facchini et al. [33]은 흡연이 심혈관계 질환의 위험성을 증가시키는 데 있어서 대사증후군이 연결요인이 되며, 이는 인슐린 저항성에 의한 것이라고 하였다. 이러한 결과는 흡연과 대사증후군이 심혈관계 질환의 위험요인으로 작용한다는 과거 연구결과와 일치한다[9,15]. 또한 대사증후군이 없는 군에서도 비흡연자에 비해 과거흡연, 현재흡연자의 비정상 경동맥 내중막 두께와 동맥경화반 위험이 증가하여, 흡연이 동맥경화증과 부분적으로 독립적인 연관성을 보였다.
본 연구는 제한점을 갖고 있다. 첫째, 건강검진 실시자를 대상으로 하여, 과거흡연자의 금연기간을 알 수 없었다. 건강상태 호전을 기대하기 위한 금연 지속기간은 누적흡연량에 비례하므로, 추가적으로 이를 반영한 결과 도출이 필요하다. 둘째, 단일 조사 시점에서 자기기입식 설문조사를 통해 흡연량과 흡연기간을 측정하여, 응답오류 및 무응답 등으로 인한 일부 데이터 손실이 발생하였다. 셋째, 단면연구로 진행된 본 연구는 흡연과 대사증후군 및 죽상동맥경화 간의 인과관계를 규명하는 데 한계가 있었다.
흡연은 대사증후군뿐만 아니라 비정상 경동맥 내중막 두께 및 동맥경화반 등 동맥경화증과 관련이 있었다. 누적흡연량이 비슷한 수준에서 과거흡연자와 현재흡연자의 질환 위험도는 비슷하였으며, 누적흡연량이 많을수록 질환위험이 높아지는 비례적 관계를 보였다. 또한 대사증후군 유무에 따라 차이를 보이는 흡연과 동맥경화증 위험도의 관계는 흡연이 동맥경화증과 부분적으로 연관성이 있음을 보여준다. 이는 흡연의 중단으로 인한 복합적인 이익효과를 설명하는 주요 근거가 된다. 그러므로 금연 후에도 지속되는 인슐린 저항성에 의한 심혈관계 질환 위험을 낮추기 위하여, 식이요법과 활동량 증가를 위한 생활습관 변화 과정이 금연 프로그램에 포함되어야 할 것으로 생각된다. 또한 흡연자에서 대사증후군의 발생은 심혈관계 질환 위험을 상승시킬 수 있으므로, 두 위험요인의 복합적 특성에 대한 추가적인 연구가 필요할 것으로 사료된다.
Figure 1.Odds ratios for r according to the smoking status. (A) abnormal carotid intima-media thickness; (B) carotid plaque. Mets, metabolic syndrome. Data are adjusted for age, body mass index, low density lipoprotein cholesterol. *p<0.05, **p<0.001. 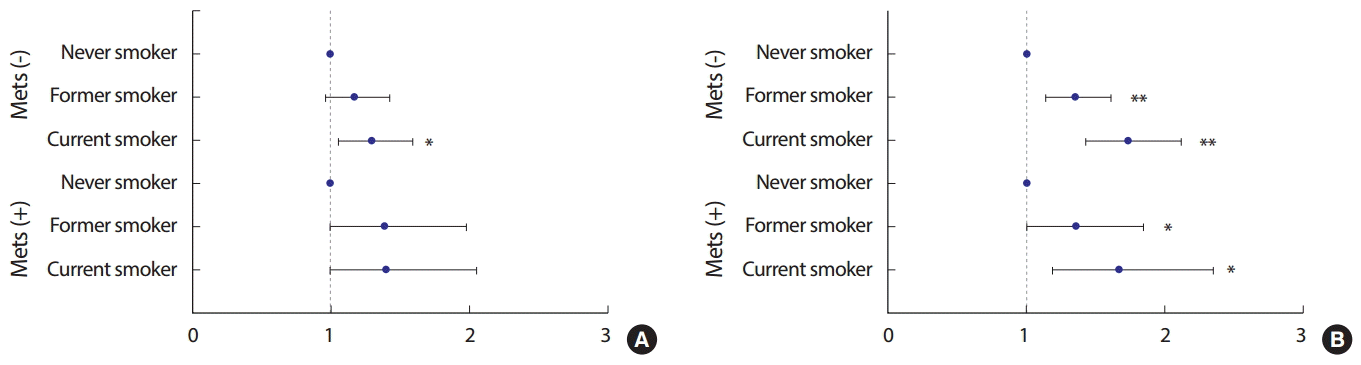
Figure 2. Odds ratios for abnormal carotid intima-media thickness according to the smoking amounts. (A) without metabolic syndrome; (B) with metabolic syndrome. PY, pack-year. Data are adjusted for age, body mass index, low density lipoprotein cholesterol. *p<0.05, **p<0.001. 
Figure 3.Odds ratios for carotid plaque according to the smoking amounts. (A) without metabolic syndrome; (B) with metabolic syndrome. PY, pack-year. Data are adjusted for age, body mass index, low density lipoprotein cholesterol. *p<0.05, **p<0.001. 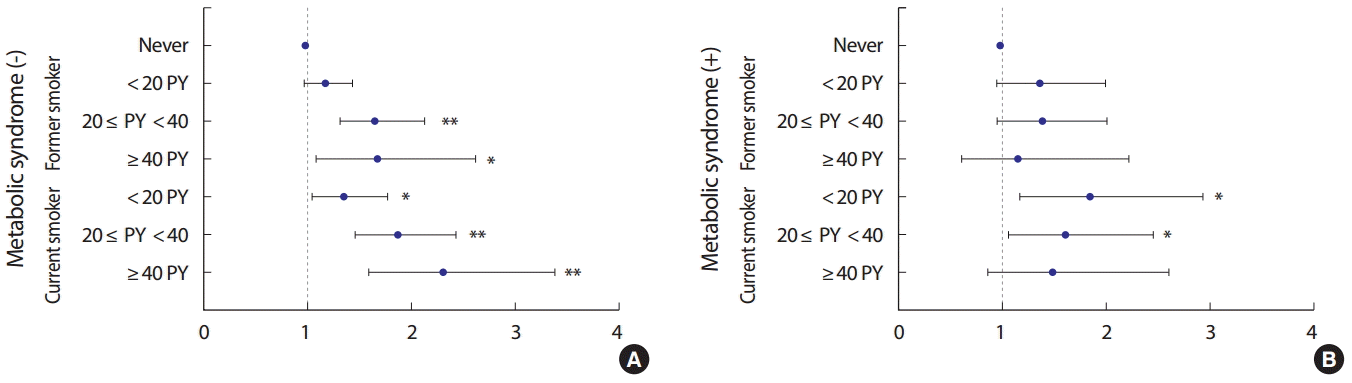
Table 1.Characteristics of subjects according to smoking status (unit: Mean ± SD)
Table 2.Logistic regression of metabolic syndrome and its risk factor components according to smoking status (unit: n (%))
Table 3.Adjusted odds ratio of metabolic syndrome and its components, abnormal carotid intima-media thickness and carotid plaque according to smoking amounts
REFERENCES1. Ambrose JA, Barua RS. The pathophysiology of cigarette smoking and cardiovascular disease. J Am Coll Cardiol 2004;43(10):1731-1737.
2. Facchini FS, Hollenbeck CB, Jeppesen J, Chen YD, Reaven GM. Insulin resistance and cigarette smoking. Lancet 1992;339(8802):1128-1130.
3. Isomaa B, Almgren P, Tuomi T, Forsén B, Lahti K, Nissén M, et al. Cardiovascular morbidity and mortality associated with the metabolic syndrome. Diabetes care 2001;24(4):683-689.
4. Kong C, Nimmo L, Elatrozy T, Anyaoku V, Hughes C, Robinson S, et al. Smoking is associated with increased hepatic lipase activity, insulin resistance, dyslipidaemia and early atherosclerosis in type 2 diabetes. Atherosclerosis 2001;156(2):373-378.
5. Reaven G, Tsao PS. Insulin resistance and compensatory hyperinsulinemia: the key player between cigarette smoking and cardiovascular disease. J Am Coll Cardio 2003;41(6):1044-1047.
6. Lee WY, Jung CH, Park JS, Rhee EJ, Kim SW. Effects of smoking, alcohol, exercise, education, and family history on the metabolic syndrome as defined by the ATP III. Diabetes Res Clin Pract 2005;67(1):70-77.
7. Lee KS, Park CY, Meng KH, Bush A, Lee SH, Lee WC, et al. The association of cigarette smoking and alcohol consumption with other cardiovascular risk factors in men from Seoul, Korea. Ann Epidemio 1998;8(1):31-38.
8. Jeppesen J, Hein HO, Suadicani P, Gyntelberg F. Low triglycerides-high high-density lipoprotein cholesterol and risk of ischemic heart disease. Arch Intern Med 2001;161(3):361-366.
9. Ishizaka N, Ishizaka Y, Toda E, Hashimoto H, Nagai R, Yamakado M. Association between cigarette smoking, metabolic syndrome, and carotid arteriosclerosis in Japanese individuals. Atherosclerosis 2005;181(2):381-388.
10. Hong AR, Lee KS, Lee SY, Yu JH. Association of current and past smoking with metabolic syndrome in men. J Prev Med Public Health 2009;42(3):160-164. (Korean).
11. Oh SW, Yoon YS, Lee ES, Kim WK, Park C, Lee S, et al. Association between cigarette smoking and metabolic syndrome: the Korea national health and nutrition examination survey. Diabetes care 2005;28(8):2064-2066.
12. Calo WA, Ortiz AP, Suárez E, Guzmán M, Pérez CM. Association of cigarette smoking and metabolic syndrome in a Puerto Rican adult population. Int J Prev Med 2013;15(4):810-816.
13. Miyatake N, Wada J, Kawasaki Y, Nishii K, Makino H, Numata T. Relationship between metabolic syndrome and cigarette smoking in the Japanese population. Intern Med 2006;45(18):1039-1043.
15. Zhang L, Guo Z, Wu M, Hu X, Xu Y, Zhou Z. Interaction of smoking and metabolic syndrome on cardiovascular risk in a Chinese cohort. Int J Cardiol 2013;167(1):250-253.
16. He Y, Lam TH, Jiang B, Wang J, Sai X, Fan L, et al. Combined effects of tobacco smoke exposure and metabolic syndrome on cardiovascular risk in older residents of China. J Am Coll Cardiol 2009;53(4):363-371.
17. Sonesson B, Ahlgren AR, Lazer L, Lanne T. Does long-term smoking affect aortic stiff ness more in women than in men? Clin Physiol 1997;17(5):439-447.
18. Grundy SM, Cleeman JI, Daniels SR, Donato KA, Eckel RH, Franklin BA. Diagnosis and management of the metabolic syndrome: an American heart association/national heart, lung, and blood institute scientific statement. Circulation 2005;112(17):2735-2752. Doi: 10.1161/CIRCULATIONAHA.105.169404
19. Lee SY, Park HS, Kim DJ, Han JH, Kim SM, Cho GJ, et al. Appropriate waist circumference cutoff points for central obesity in Korean adults. Diabetes Res Clin Pract 2007;75(1):72-80.
20. Nakanishi N, Takatorige T, Suzuki K. Cigarette smoking and the risk of the metabolic syndrome in middle-aged Japanese male office workers. Ind Health 2005;43(2):295-301.
21. Wada T, Urashima M, Fukumoto T. Risk of metabolic syndrome persists twenty years after the cessation of smoking. Intern med 2007;46(14):1079-1082.
22. Chen CC, Li TC, Chang PC, Liu CS, Lin WY, Wu MT, et al. Association among cigarette smoking, metabolic syndrome, and its individual components: the metabolic syndrome study in Taiwan. Metabolism 2008;57(4):544-548.
23. Oh JE. Association between smoking status and metabolic syndrome in men. Korean J Obes 2014;23(2):99-105. (Korean).
24. Will JC, Galuska DA, Ford ES, Mokdad A, Calle EE. Cigarette smoking and diabetes mellitus: evidence of a positive association from a large prospective cohort study. Int J Epidemiol 2001;30(3):540-546.
25. Kim HJ, Kim JS, Yoo JH. Association between smoking status and insulin resistance in apparently healthy Korean men. Korean J Fam Med 2009;30(3):190-196. (Korean).
26. Matsushita Y, Nakagawa T, Yamamoto S, Takahashi Y, Noda M, Mizoue T. Associations of smoking cessation with visceral fat area and prevalence of metabolic syndrome in men: the Hitachi health study. Obesity 2011;19(3):647-651.
27. Song YM, Chang WD, Hsu HY, Chen MD. A short-term smoking cessation may increase the risk of developing metabolic syndrome. Diabetes Metab Syndr 2015;9(2):135-137. Doi: 10.1016/j.dsx.2015.02.005. Epub 2015 Mar 6
28. Zhu Y, Zhang M, Hou X, Lu J, Peng L, Gu H, et al. Cigarette smoking increases risk for incident metabolic syndrome in Chinese men-Shanghai diabetes study. Biomed Environ Sci 2011;24(5):475-482. Doi: 10.3967/0895-3988.2011.05.004
29. Eliasson B, Attvall S, Taskinen MR, Smith U. The insulin resistance syndrome in smokers is related to smoking habits. Arterioscler Thromb 1994;14(12):1946-1950.
30. Nakanishi N, Nakamura K, Matsuo Y, Suzuki K, Tatara K. Cigarette smoking and risk for impaired fasting glucose and type 2 diabetes in middle-aged Japanese men. Ann Intern Med 2000;133(3):183-191.
31. Rohleder N, Kirschbaum C. The hypothalamic-pituitary-adrenal (HPA) axis in habitual smokers. Int J Psychophysiol 2006;59(3):236-243.
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||