국내 코로나19백신 안전성 모니터링을 위한 특별관심이상사례 배경발생률
Background Rates of Adverse Events of Special Interest for COVID-19 Vaccine Safety Monitoring in South Korea
Article information
Trans Abstract
Objectives
This study aimed to estimate background incidence rates (IR) for adverse events of special interest (AESI) associated with COVID-19 vaccines in South Korea.
Methods
We used data from the Korean National Health Insurance Service-National Sample Cohort from January 1, 2015 to December 31, 2019, with IR calculated annually. Eight AESIs including acute myocarditis, acute pericarditis, acute disseminated encephalomyelitis (ADEM), acute transverse myelitis (ATM), encephalitis, anaphylaxis, Bell's palsy, and lymphadenitis were evaluated. Two operational strategies were implemented: a broad definition using ICD-10 codes for primary or secondary diagnoses to enhance sensitivity, and a narrow definition integrating ICD-10 codes with procedure and drug codes for enhanced accuracy and specificity. IR was calculated by dividing the number of incident cases by the total person-time at risk, with separate analyses by sex and age.
Results
During the study period, the incidence of anaphylaxis, Bell's palsy, and lymphadenitis under the broad definition continued to increase. Under the narrow definition, there were no reported cases of acute myocarditis or Bell's palsy from 2015 to 2019. Additionally, the incidence rates for acute pericarditis, ADEM, ATM, encephalitis, anaphylaxis, and lymphadenitis were lower than those calculated under the broad definition. Males generally had higher rates, except for Bell's palsy and lymphadenitis. Most AESIs were more common in individuals aged 65 and older, whereas ADEM and lymphadenitis were higher in children aged 0-19 years.
Conclusions
Variability in AESI rates emphasizes the importance of considering definitions and demographics when establishing background rates for surveillance, which is a critical aspect of monitoring vaccine safety.
서 론
전 세계적으로 코로나19 감염 및 전파를 예방하기 위해 코로나19백신 접종을 시작하면서 백신 개발 단계에서 확인되지 않았던 다양한 종류의 이상사례가 보고되었다. 이상사례가 코로나19백신 접종과의 관련성이 충분히 입증되지 않았음에도 이상사례로 보고된 사례는 국민들에게 불안감을 조성하여 백신 접종을 망설이거나 주저하게 하였다. 따라서 코로나19백신 접종 전 이상사례의 배경발생률(background rate)을 산출하여 예방접종 후 이상사례의 발생률과 비교하여 코로나19백신 접종이 잠재적인 위험을 증가시켰는지 확인하는 것이 필요하다. 배경발생률은 코로나19백신과 같은 특별한 개입이 없을 때 자연적으로 발생하는 각 질환의 발생률을 지칭한다.
미국에서 백신 능동적 감시를 수행하는 센티넬 이니셔티브(Sentinel Initiative)의 Biologics Effectiveness and Safety (BEST) 이니셔티브와 유럽의 vACCine Covid-19 monitoring readinESS (ACCESS) 프로젝트에서는 코로나19백신의 안전성을 모니터링하기 위해 특별관심이상사례(adverse events of special interest, AESI) 목록을 선정한 후 배경발생률 연구를 수행하였다[1-3]. 캐나다에서도 코로나19백신과 관련된 11가지 AESI에 대한 배경발생률을 추정하여 안전성 감시를 수행하였다[4]. AESI는 대유행 예방접종에 있어 보건의료 및 공중보건 영역에서 의미 있는 이상사례를 의미하며, 백신 안전성을 모니터링하고 평가하는 데 활용된다. 코로나19백신 시판 후 안전성 문제에 대비하기 위해서는 코로나19백신 접종 시 나타날 수 있는 AESI 목록을 선정하여 배경발생률 연구를 수행해야 하며, 코로나19백신과 관련한 이상사례를 지속적으로 감시해야 한다.
코로나19백신 접종 전 AESI의 배경발생률 추정하여 예방접종 후 자료와 비교를 통해 예방접종이 잠재적 위험을 증가시키는지 확인하는 것은 코로나19백신과 이상사례 간 인과관계를 해석하는데 도움이 된다. 한국에서는 국내외 이상반응 보고시스템에 많이 보고되고 임상시험 중 잠재적 인과성이 제기된 아나필락시스(anaphylaxis), 급성파종성뇌척수염(acute disseminated encephalomyelitis, ADEM), 벨마비(Bell's palsy), 횡단성척수염 등 주요 11가지 질환에 대해 배경발생률을 산출한 선행연구가 있다[5]. 또한, 아스트라제네카(AstraZeneca) 백신 접종 초기에 제기된 혈전 관련 질환과[6] 심근염, 심낭염 등 코로나19백신 접종과 관련된 13가지 질환에 대한 지난 10년간 발생 현황을 보고한 연구가 있다[7]. 하지만 청구자료를 활용한 국내 AESI에 관한 배경발생률 연구는 처치 및 치료약제를 고려하는 등 보다 엄격한 조작적 정의를 활용한 연구는 제한적이다. 청구자료는 진료비 청구 목적으로 수집된 자료로 질병코드만 이용하여 환자를 선별하는 경우에 질환 발생이 과대 추정될 가능성이 있다[8]. 따라서 각 질환의 상태에 따라 다양한 중등도와 원인을 감별할 수 있도록 질병코드와 처치 및 치료약제 코드를 조합하여 조작적 정의를 내리는 것이 필요하다. 또한, 소아청소년, 청년층, 장년층, 노인층에 대한 결과와 성별에 관한 배경발생률 연구는 찾아보기 어려워 관련 연구가 필요하다.
본 연구는 한국에서 AESI 중 주요하게 논의된 급성심근염, 급성심낭염, ADEM, 급성횡단척수염(acute transverse myelitis, ATM), 뇌염, 아나필락시스, 벨마비, 림프절염에 대해 연도별, 성별, 연령대별 국내 배경발생률을 파악하고자 한다. 이를 통해 해당 질환의 발생 예측과 실제 질환 발생 현황의 비교를 위한 기초자료로 활용하고자 한다.
연구 방법
연구자료 및 대상
본 연구의 자료원은 국민건강보험공단 표본코호트 2.2 자료로, 한국의 건강보험체계하에서 전 국민을 대표하며 질환의 시계열적 발생 경향을 파악할 수 있다. 연구기간은 국내 코로나19백신 접종 전 기간으로 2015년 1월 1일부터 2019년 12월 31일까지이며, 매년 각 질환의 발생률을 산출하였다.
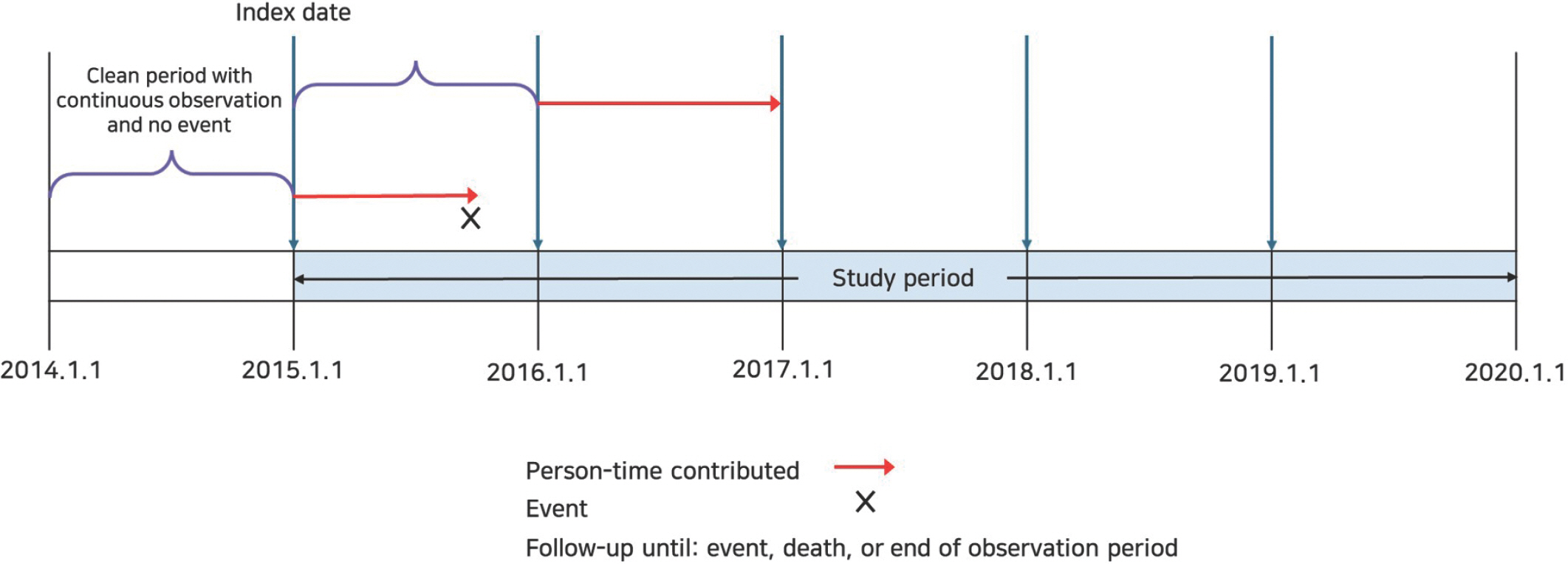
연구대상자는 2006년 1년간 건강보험가입자 혹은 의료급여수급권자 자격을 유지한 100만 명이다. 코호트 입적일(index date)은 매년 1월 1일로 설정하였으며, 환자는 코호트 입적일 이전 사정 지정된 클린윈도우(clean window) 기간에 AESI 진단이 없고 계속 등록되어 있어야 한다. 클린윈도우 기간은 코호트 입적일 전 기간으로 정의하며, 이 기간 동안 AESI가 관찰되지 않아야 한다. AESI는 국내 코로나19백신 접종과 관련이 있을 수 있는 질환이고 최근 국내외 AESI를 고려하여 총 8가지 질환(급성심근염, 급성심낭염, ADEM, ATM, 뇌염, 아나필락시스, 벨마비, 림프절염)을 선정하였다. 클린윈도우 기간은 미국 Food and Drug Administration (FDA) 프로토콜을 따라 아나필락시스(30일), 뇌염(183일), 벨마비(183일)를 제외한 질환은 365일로 설정하였다[2]. 본 연구의 디자인은 Figure 1과 같다.
질환의 조작적 정의
각 AESI의 조작적 정의는 배경발생률과 관련한 FDA, ACCESS, Global Vaccine Data Network (GVDN)의 프로토콜을 종합하여 정리하였으며, 넓은(broad) 정의와 좁은(narrow) 정의로 구분하여 정의하였다. 넓은 정의는 민감도를 높이기 위해 제10차 국제질병분류(International Classification of Diseases 10th Revision, ICD-10)를 이용하여 사전 정의된 질병코드가 주상병 및 제1부상병까지 기재된 경우 해당 질환이 발생한 것으로 정의하였다. 좁은 정의는 정확도와 특이도를 높이기 위해 ICD-10 코드와 처치 또는 치료약제 코드를 조합하여 사전 정의된 코드가 모든 상병에 기재된 경우 해당 질환이 발생한 것으로 정의하였다. 하지만, 급성심낭염의 경우 주상병 및 제1부상병에서보다 모든 상병을 포함한 경우에 더 많이 관찰되어 민감도를 높이는 넓은 정의를 모든 상병에서 급성심낭염으로 진단받았으면서 혈액 검사인 C-반응성 단백질 또는 적혈구 침강 속도 또는 영상 검사 이력이 있는 입원 환자로 정의하였고, 좁은 정의는 주상병 및 제1부상병으로 급성심낭염으로 진단받은 자로 정의하였다. 림프절염은 질병코드로만 넓은 정의와 좁은 정의를 정의하였으며, 넓은 정의는 모든 상병에서 림프절염 관련 진단명이 있는 자로 정의하였고, 좁은 정의는 주상병 및 제1부상병에서 관련 질병코드가 있는 자로 정의하였다(Supplementary Table 1).
통계분석
연구대상자는 코호트 입적일부터 AESI 발생, 사망, 연도 말 중 가장 처음에 발생한 사건까지 추적 관찰되었다. 클린윈도우 기간이 365일 미만인 질환이면 동일한 연도에 재진입이 가능하며, 재진입한 개인은 별도의 관찰 사례로 간주하였다. 발생률(incidence rate, IR)은 분모에 인-시(person-time)를 기여한 개인 중 발생 사례 수를 총 person-time at risk로 나누어 계산하였으며, 10만 인년(person-years)당으로 표시하였다. Person-time at risk는 코호트 입적일부터 추적 관찰 기간 및 중도 절단 날짜까지의 개인 인-시로 정의하였다. 연도별, 성별, 연령대에 따라 각 AESI의 발생률과 95% 신뢰구간을 계산하였다. 통계 분석은 SAS 9.4 (SAS Institute Inc., Cary, NC, USA)를 사용하였으며, 그래프의 시각화는 R version 4.2.2의 ggplot2 version 3.4.2 package를 사용하여 작성하였다. 본 연구는 이화여자대학교 임상연구심의위원회의 심의면제(IRB No.: ewha-202304-0022-01)를 받아 진행하였다.
연구 결과
연도별 특별관심이상사례 발생률
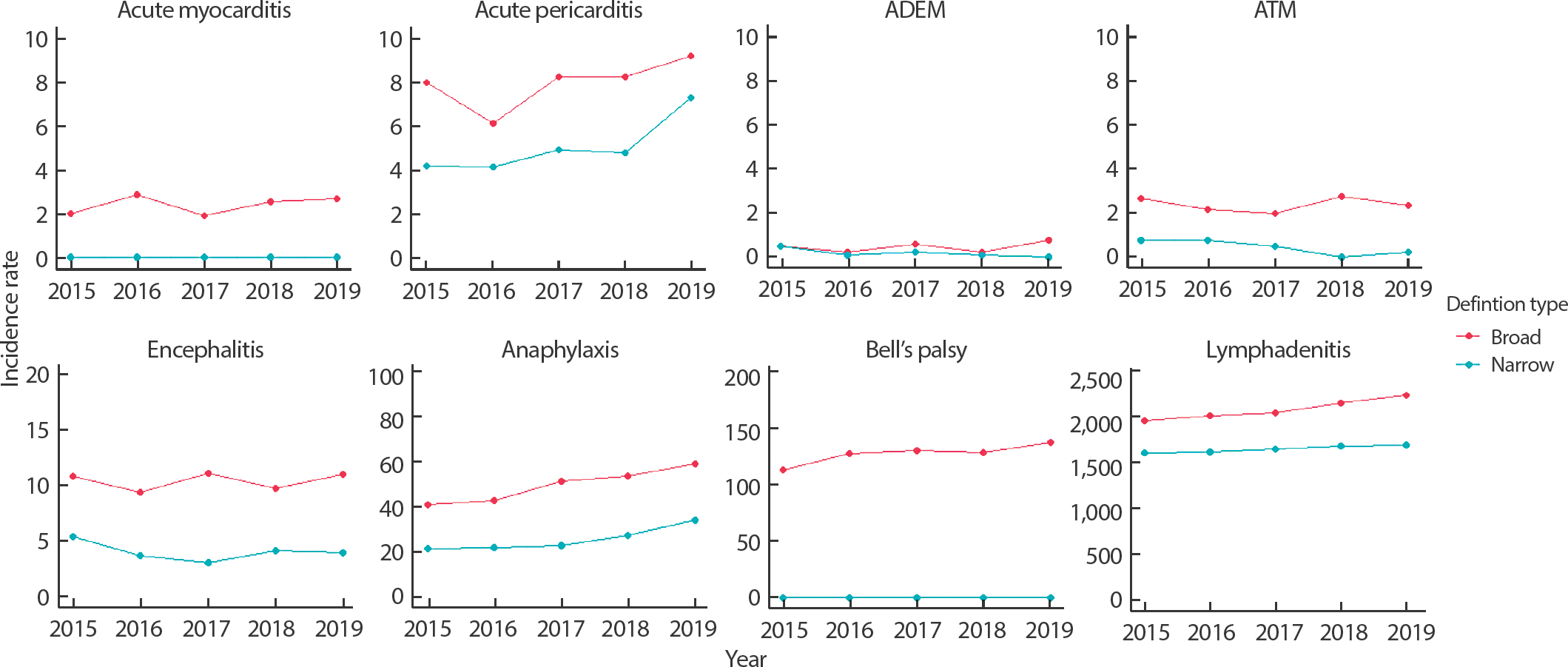
급성심근염은 넓은 정의에서 2015년부터 2019년까지 안정한 추세를 보였으나, 좁은 정의에서는 연구기간 동안 발생 건수가 0으로 연도별 발생률을 확인할 수 없었다. 급성심낭염은 넓은 정의에서 좁은 정의에 비해 발생률이 높게 나타났으며, 좁은 정의에서 연도에 따라 증가하는 경향성을 보여주었다. ADEM과 ATM은 넓은 정의와 좁은 정의에서 연구기간 동안 안정적인 추세를 보였으며, 좁은 정의에서 넓은 정의에 비해 연도별 발생률이 낮게 나타났다. 뇌염은 넓은 정의에서 좁은 정의에 비해 발생률이 높게 나타났으며, 연도별 비슷한 발생률이 관찰되었다. 아나필락시스는 넓은 정의에서 좁은 정의에 비해 연도별 발생률이 높게 나타났으며, 연도에 따라 증가하는 경향성을 관찰하였다. 벨마비는 넓은 정의에서 연도에 따라 발생률이 증가하는 경향성을 보여주었으나, 좁은 정의에서는 연구기간 동안 발생 건수가 0으로 발생률을 확인할 수 없었다. 림프절염은 넓은 정의에서 좁은 정의에 비해 연도별 발생률이 높게 나타났으며, 연도에 따라 증가하는 경향성을 관찰하였다(Figure 2).
연도별 성별 특별관심이상사례 발생률
Figure 3A는 넓은 정의를 기준으로 한 각 질환의 연도별 성별 발생률을 나타낸다. 급성심근염, ATM은 모든 연도에서 남성이 여성보다 발생률이 높게 나타났다. 급성심낭염은 대체로 남성과 여성 간 큰 차이가 없었으나 2019년에는 남성이 여성보다 발생률이 높게 나타났다. ADEM은 대체로 남성과 여성 간 큰 차이가 없었으나 2017년에는 여성이 남성보다 발생률이 높았다. 뇌염은 2018년 이후부터 지속해서 여성이 남성보다 발생률이 높게 관찰되었다. 아나필락시스는 2015년부터 2018년까지 남성이 여성보다 발생률이 높다가, 2019년부터 여성의 발생률이 더 높아졌다. 벨마비와 림프절염은 모든 연도에서 여성이 남성보다 발생률이 높게 나타났다.
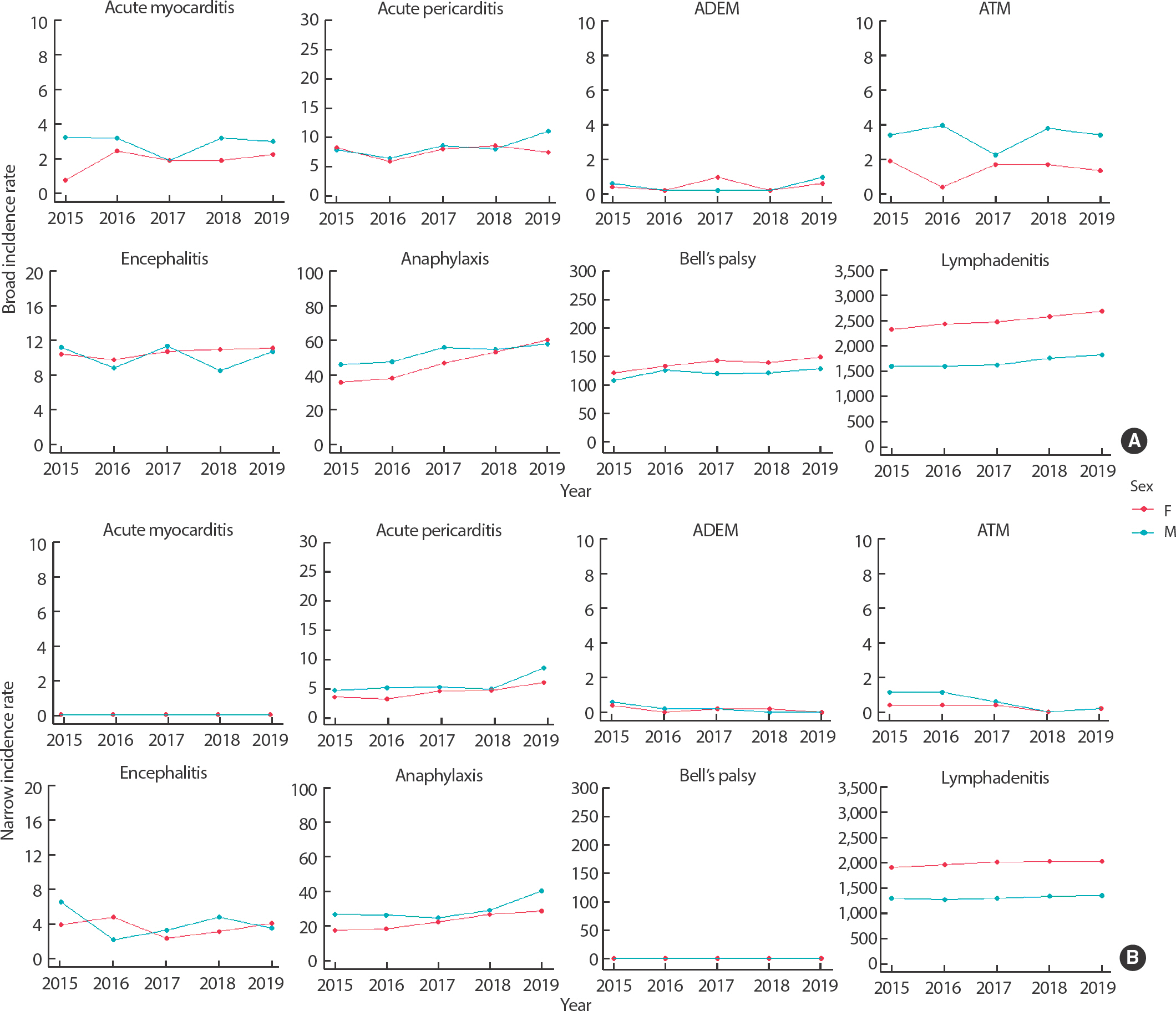
Annual incidence rates per 100,000 person-years for 8 adverse events of special interest in South Korea by sex. (A) Broad definition. (B) Narrow definition. ADEM, acute disseminated encephalomyelitis; ATM, acute transverse myelitis.
좁은 정의를 기준으로 분석한 결과(Figure 3B), 급성심근염과 벨마비는 연구기간 동안 발생 건수가 0으로 발생률을 확인할 수 없었다. 급성심낭염은 모든 연도에서 남성이 여성보다 발생률이 높게 나타났다. ADEM, ATM, 뇌염은 대체로 남성이 여성보다 발생률이 높게 나타났다. 아나필락시스는 모든 연도에서 남성이 여성보다 발생률이 높게 관찰되었다. 림프절염은 모든 연도에서 여성이 남성보다 발생률이 높게 나타났다.
연도별 연령대별 특별관심이상사례 발생률
Figure 4A는 넓은 정의를 기준으로 한 각 질환의 연도별 연령대별 발생률을 나타낸다. 급성심근염은 2015년에 20-29세 연령대에서 10만 인년당 4.34명으로 가장 높은 발생률을 보였으며, 연령대에 따른 발생률은 연도별로 다양하게 관찰되었다. 급성심낭염은 모든 연도에서 65세 이상 연령대에서 발생률이 높게 나타났다. ADEM은 모든 연도에서 20-29세 연령대에서는 질병 발생이 관찰되지 않았으며, 다른 연령대와 비교하여 0-19세 연령대에서 발생률이 높게 나타났다. ATM은 2015년에 65세 이상 연령대에서 10만 인년당 5.7명으로 가장 높은 발생률이 관찰되었으며, 모든 연도에서 65세 이상 연령대의 발생률이 높게 관찰되었다. 뇌염은 모든 연도에서 0-19세 연령대와 65세 이상 연령대에서 발생률이 높게 나타났다. 아나필락시스와 벨마비는 연령이 증가할수록 발생률이 증가하는 경향성을 보였으며, 65세 이상 연령대에서 발생률이 높게 나타났다. 림프절염은 연령이 낮을수록 발생률이 높았으며, 모든 연도에서 0-19세 연령대의 발생률이 가장 높았다.
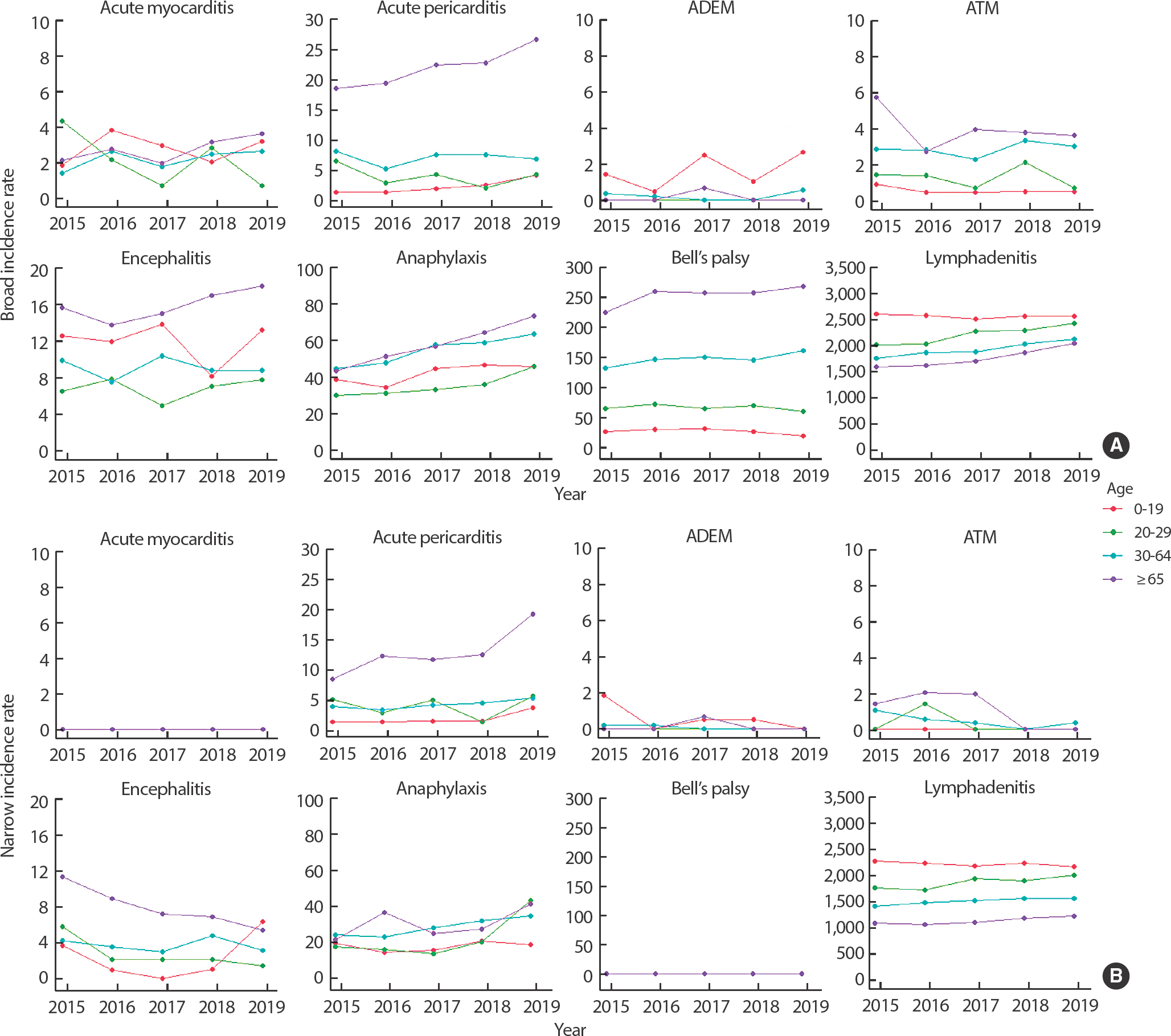
Annual incidence rates per 100,000 person-years for 8 adverse events of special interest in South Korea by age group. (A) Broad definition. (B) Narrow definition. ADEM, acute disseminated encephalomyelitis; ATM, acute transverse myelitis.
좁은 정의를 기준으로 분석한 결과(Figure 4B), 급성심근염과 벨마비는 연구기간 동안 발생 건수가 0으로 발생률을 확인할 수 없었다. 급성심낭염은 넓은 정의와 유사하게 모든 연도에서 65세 이상 연령대에서 발생률이 높게 관찰되었다. ADEM은 넓은 정의와 동일하게 20-29세 연령대에서 발생 건수가 0으로 발생률을 확인할 수 없었으며, 다른 연령대와 비교하여 0-19세 연령대에서 발생률이 높게 관찰되었다. ATM 은 모든 연도에서 0-19세 연령대에서 질병의 발생이 관찰되지 않았으며, 65세 이상 연령대에서 발생률이 높게 나타났다. 뇌염과 아나필락시스는 대체로 65세 이상 연령대에서 발생률이 높게 관찰되었다. 림프절염은 넓은 정의와 유사하게 연령이 낮을수록 발생률이 높았으며, 모든 연도에서 0-19세 연령대 발생률이 가장 높게 나타났다.
고 찰
본 연구는 국민건강보험공단 표본코호트 2.2 자료를 기반으로 코로나19백신 접종과 관련된 주요 8가지 질환에 대해 2015년부터 2019년까지 연도별, 성별, 연령대별 발생률을 제시하였다. 새로운 백신이 도입될 경우 해당 백신 접종 후 발생할 수 있는 질환의 배경발생률을 파악하는 것은 중요하다. 배경발생률은 위험 증가 또는 안전 우려를 식별하기 위한 능동적 감시 연구에서 사용되며, 예방접종 후 인구집단에서 관찰된 비율과 비교하여 예상되는 AESI 발생률을 추정하는 데 활용될 수 있다.
본 연구에 이용한 각 질환의 조작적 정의는 관련 선행연구를 종합하여 정리하였다. 각 질환의 다양한 중등도와 원인을 감별하기 위해 질병코드를 이용한 넓은 정의와 처치 및 치료약제 코드를 함께 활용한 좁은 정의, 총 두 가지의 조작적 정의를 이용하였다. 급성심근염은 좁은 정의에서 발생 건수가 관찰되지 않았으며, 넓은 정의에서는 연구기간 동안 10만 인년당 1.89-2.83명으로 발생률이 추정되었다. 질병코드만을 활용하여 국내 심근염 발생률을 산출한 선행논문에서는 10만 명당 0.55-1.38명의 발생률이 추정되었다[9]. 급성심낭염은 좁은 정의와 넓은 정의에서 모두 2019년 가장 높은 발생률이 추정되었다. 2018년도와 2019년도가 동일한 발생률이 산출되었던 선행연구와는 다른 결과를 보였지만 이는 질환 정의 및 자료의 차이로 인한 결과일 수 있다[9]. ADEM은 연구기간 동안 넓은 정의와 좁은 정의에서 발생률이 각각 10만 인년당 0.19-0.75명, 0.09-0.47명으로 발생률이 매우 낮게 추정되었으며, 이는 선행연구와 일치한다[5]. ADEM은 상대적으로 희귀한 질환이고 진단이 어려운 경우가 많아 발생률이 낮게 나타난 것으로 생각된다. ATM은 드물게 발생하는 질환으로 연구기간 동안 넓은 정의는 10만 인년당 1.98-2.73명, 좁은 정의는 10만 인년당 0.19-0.76명의 발생률이 산출되었다. 넓은 정의의 발생률 결과는 미국에서 횡단성 척수염 발생률을 산출한 선행연구와 유사하였다[10]. 뇌염은 넓은 정의에서 좁은 정의에 비해 연도별 발생률이 높게 관찰되었는데, 넓은 정의와 좁은 정의 간에 발생률 차이가 나타나는 것은 질병 범주의 포괄성, 진단 기준의 엄격성 등 다양한 요인에 대해 영향을 받아 나온 결과라 생각된다. 아나필락시스는 넓은 정의와 좁은 정의를 활용한 두 결과 모두에서 지속적으로 발생률이 증가하는 양상을 보여주었다. 이는 이전 연구 결과와 일치하며[5,11], 본 연구에서 전체적으로 발생률이 더 높게 관찰되었다. 시간이 지남에 따라 질환의 발생률이 증가하는 것은 질환 인지율 증가, 새로운 진단 기준 적용, 환자들의 의료 서비스 접근성 향상과 관련될 수 있을 것으로 생각된다. 벨마비는 넓은 정의에서 발생률이 지속적으로 증가하였으며, 이는 질병코드를 이용하여 벨마비 발생률을 확인한 이전 선행연구 결과와 유사하다[5]. 또한, 진단 및 치료약제 코드를 활용하여 벨마비 발생률을 확인한 연구에서도 2008년 10만 명당 23.0명에서 2018년 10만 명당 30.8명으로 증가하는 추세를 보여주었으나[12], 본 연구의 좁은 정의에서는 연구기간 동안 발생 건수가 0으로 발생률을 확인할 수 없었다. 림프절염은 넓은 정의와 좁은 정의에서 지속적으로 발생률이 증가하는 양상을 보여주었다.
코로나19백신 접종과 관련된 8가지 질환에 대한 각각의 배경발생률은 성별 및 연령대에 따라 다양하게 나타났다. 벨마비와 림프절염을 제외한 대부분의 질환에서 남성이 여성보다 발생률이 높게 나타났다. 65세 이상 노인은 급성심낭염과 뇌염의 발생률이 연구기간 동안 높게 관찰되었다. 뇌염은 주요 호발 연령대가 10세 미만 아동과 50-60대 장년층으로 보고되고 있으며[13], 이는 본 연구 결과와 유사하다. 아나필락시스와 벨마비는 연령이 증가할수록 발생률이 높았으며, 이는 한국에서 아나필락시스 발생률 추세에 대한 이전 선행연구의 성별 및 연령에 따른 발생 양상과 일치한다[11]. 0-19세 소아청소년은 ADEM과 림프절염 발생률이 높게 나타났다. ADEM과 관련하여 중국에서 수행한 선행연구에서도 10세 미만에서 가장 발생률이 높아 주로 어린이에서 많이 발병한다는 점에서 본 연구의 결과와 유사하며 성별 발생 양상 또한 일치하였다[14]. 림프절염과 관련하여 단면연구를 수행한 연구에서도 10대 청소년에게 림프절염이 자주 발생하였으며[15], 이는 본 연구 결과와 일치한다.
본 연구는 최근 국내외 AESI 목록과 코로나19백신 접종과 관련이 있는 질환을 고려하여 최종 분석 질환을 선정하였다. 하지만 본 연구에서 분석한 질환 외에도 mRNA (messenger ribonucleic acid) 백신, 아데노바이러스 벡터(adenovirus vector) 백신 등 코로나19백신 종류별 주요 이상사례에 대한 배경발생률 연구를 수행하는 것이 필요하다. 아스트라제네카 백신이나 얀센(Janssen) 백신과 같은 아데노바이러스 벡터 백신의 경우, 백신 접종 후 매우 드물게 길랑-바레 증후군(Guillain‐ Barre syndrome)과 혈소판 감소성 혈전증(thrombosis with thrombocytopenia syndrome)이 보고되었다[16-18]. mRNA 백신 접종에 관한 체계적 문헌고찰 연구에서는 백신 접종 후 혈전증이 가장 많이 보고되었으며, 다음으로 뇌졸중, 심근염, 심근경색, 폐색전증 순으로 나타났다[19]. mRNA 백신은 특히 젊은 남성에서 백신 접종 후 심근염 및 심낭염이 발생한 것이 보고되었다[20,21]. 이처럼 코로나19백신 종류별로 나타날 수 있는 주요 이상사례에 대한 배경발생률을 산출하여, 코로나19백신 접종 후 보고된 이상사례를 잘 이해하고 시판 후 안전성 평가의 근거를 마련하는 것이 필요하다. 즉, AESI로 간주되는 질환의 배경발생률을 백신 접종 전 산출하여 접종 후 감시자료와 비교하여 백신 접종이 잠재적인 위험을 증가시키는지 확인하는 과정이 중요하다.
백신 안전성 감시를 위한 배경발생률을 산출할 때 특정 질환을 가진 환자를 가장 잘 추출하는 조건인 조작적 정의를 적절히 정의하는 것은 중요하다. 실제 질환을 가진 환자를 얼마나 정확히 식별하는지의 정도가 연구의 신뢰도를 결정하는 중요한 요인이 될 수 있다. 따라서 배경발생률을 추정함에 있어 이용되는 자료원에 따라 적절한 조작적 정의를 정의하는 것이 필요하다. 본 연구에서 활용한 국민건강보험공단 청구자료는 실제 진단과 다른 상병이 기록되거나 상병을 입력할 때 발생하는 오류 등으로 상병이 환자의 실제 상태를 정확하게 반영하지 못할 수 있다[8]. 또한, 자세한 검사 내역은 확인할 수 없어 자료 내에서 이용 가능한 기초 정보, 질병코드, 검사 및 시술 코드, 약제 등의 정보를 최대한 활용하여 환자를 선별하는 것이 필요하다. 본 연구에서는 질병코드를 활용해 민감도를 높인 넓은 정의와 질병코드와 처치 및 치료약제 코드를 조합해 정확도와 특이도를 높인 좁은 정의로 질환을 조작적으로 정의함으로써 연구 결과의 신뢰성을 높이고자 하였다.
백신과 이상사례 사이의 인과관계에 대한 비뚤린 판단 때문에 백신 접종률이 감소하는 것을 개선하기 위해서는 보고된 백신 이상사례에 대한 정확한 해석이 요구되며, 이를 위해 이상사례 관한 배경발생률이 필요하다[22]. 한 예로 오스트리아에서 자궁경부암 백신 도입 직후 10대 청소년의 사망이 보고되면서 백신 중단 요청이 제기된 적이 있다. 하지만 청소년 돌연사에 대한 배경발생률 값이 제공된 후 문제의 발생률과 청소년 돌연사의 배경발생률을 비교하여 백신의 안전성을 평가하였고, 결과적으로 백신 접종 프로그램을 계속 진행하였다[23,24]. 이처럼 백신 접종 후 나타날 수 있는 이상사례에 관한 배경발생률은 백신 접종과 이상사례 간의 인과관계를 평가하는 데 중요한 기준이 된다. 따라서 백신의 시판 후 안전성 감시에 있어서 이상사례의 배경발생률을 산출하여 추가적인 안전성 조사 판단 기준 및 인과관계 평가의 근거를 마련하는 것이 중요하다[25]. 또한, 인구특성별 배경발생률은 능동적 안전성 감시에서 적절한 비교 대상을 선정하는 데 도움이 될 수 있다.
본 연구는 몇 가지 장점과 의의가 있다. 첫째, 한국인을 대상으로 코로나19백신 접종 후 나타날 수 있는 주요 8가지 질환에 대해 성별 및 연령대별로 세분화하여 발생률을 확인하였다(Supplementary Tables 2-6). 둘째, 전 국민을 대표하며 다양한 질환의 발생 경향을 감지할 수 있는 자료원을 이용하였다. 셋째, 성별 및 연령대에 따른 발생률 차이를 연구함으로써 코로나19백신 안전성 모니터링 및 공중보건 정책 발전에 기여할 수 있다. 넷째, 각 AESI의 조작적 정의를 넓은 정의와 좁은 정의로 구분한 연구결과를 각각 제시함으로써, 조작적 정의에 따른 발생률 차이를 확인하였다. 넓은 정의를 이용하면 보다 포괄적으로 잠재적인 이상사례를 포착할 가능성이 높아 초기 스크리닝 및 역학 감시에 사용하는 것이 유용하다고 생각된다. 인과관계를 규명하거나 특정 개입의 영향을 평가하는 등 정확도가 중요한 연구에서는 좁은 정의를 이용하는 것이 적절할 수 있다고 생각된다.
하지만 연구 결과를 살펴보았을 때, 몇 가지 제한점이 있다. 첫째, 본 연구는 표본 추출된 100만 명을 대상으로 하여 드물거나 희귀한 질환인 경우 발생이 관찰되지 않을 가능성이 있다. 추후 연구에서는 이러한 제한점을 고려하여 적절한 자료원과 조작적 정의를 이용하여 연구를 수행하는 것이 필요하다. 둘째, 국민건강보험공단 자료는 요양기관에 건강보험 및 의료급여 지급을 목적으로 축적된 자료로 일부 진단명이 부정확할 수 있다. 이에 본 연구에서는 질병코드만 사용해서는 질환의 진단명 타당성을 확보하는 데 한계가 있을 수 있어, 처치 및 치료약제 코드를 활용한 연구 결과도 함께 제시하여 진단명 타당성을 확보하고자 노력하였다. 셋째, mRNA 백신, 아데노바이러스 벡터 백신 등 코로나19백신 종류별 주요 이상사례를 포함하지 못하였다. 넷째, 성별 및 연령대별로 세분화한 연구 결과를 산출하였으나, 성별과 연령을 교차분석한 연구는 수행하지 못하였다. 향후 연구에서는 성별과 다른 사회적 범주(연령, 장애, 소득 등)의 교차에 따라 결과에 어떤 차이가 있는지 분석하는 것이 필요하다. 마지막으로 만성질환자(당뇨병, 비만, 만성폐쇄성폐질환 등), 면역저하자 등 코로나19 감염에 취약하거나 중증 감염의 위험이 높은 환자에 대한 배경발생률을 조사하지 못하였다. 국내 코로나19 고위험군의 배경발생률은 해당 집단에서 위험 증가 또는 안전 우려를 식별하기 위한 기초자료가 되며, 코로나19 고위험군을 대상으로 배경발생률에 관한 연구가 필요하다.
결 론
본 연구는 코로나19백신 접종과 관련한 주요 8가지 질환에 대해 코로나19백신 접종 이전인 2015년부터 2019년까지 연도별, 성별, 연령대별 발생률을 제시하였다. 코로나19백신처럼 새로운 백신이 도입되는 상황에서 이상사례의 배경발생률을 파악하는 것은 백신 안전성 모니터링에서 중요한 역할을 한다. 또한, 백신 안전성 감시를 위해서는 성별, 연령별 등 인구특성에 따라 구분된 배경발생률을 산출하여 접종 후 감시자료와 비교를 통해 백신 접종이 위험을 증가시켰는지 확인할 필요가 있다. 이러한 접근은 백신과 이상사례 사이의 인과관계를 해석하는데 도움이 되며 인과성 평가의 근거가 될 수 있다.
Supplementary Materials
Supplementary Table 1.
The list of conditions included in the study and the ICD-10 codes used to capture their incidences
Supplementary Table 2.
Annual incidence rates per 100,000 person-years for 8 adverse events of special interest in South Korea
Supplementary Table 3.
Annual incidence rates per 100,000 person-years for 8 adverse events of special interest in South Korea by sex based on broad definition
Supplementary Table 4.
Annual incidence rates per 100,000 person-years for 8 adverse events of special interest in South Korea by sex based on narrow definition
Supplementary Table 5.
Annual incidence rates per 100,000 person-years for 8 adverse events of special interest in South Korea by age group based on broad definition
Supplementary Table 6.
Annual incidence rates per 100,000 person-years for 8 adverse events of special interest in South Korea by age group based on narrow definition